Хронический миелобластный лейкоз – Диагностика и лечение
Хронический миелобластный лейкоз (хронический миелоидный лейкоз или миелоцитарный лейкоз, хронический миелолейкоз, ХМЛ) – болезнь, при которой наблюдается избыточное образование гранулоцитов в костном мозге и повышенное накопление в крови как самих этих клеток, так и их предшественников.
Иными словами, основу опухоли составляют клетки-предшественники миелопоэза, выросшие, но неправильно дифференцированные. Период полужизни гранулоцита ХМЛ превышает таковой нормального гранулоцита в 10 раз.
Слово «хронический» в названии болезни означает, что процесс развивается сравнительно медленно, в отличие от острого лейкоза, а «миелоидный» означает, что в процесс вовлечены клетки миелоидной (а не лимфоидной) линии кроветворения.
Хронический миелолейкоз – это наиболее распространённый вид лейкозов, на его долю приходится в среднем 20% случаев всех гемобластозов у взрослых и около 5% – у детей.
Основными методами исследования и диагностики ХМЛ в наше время остаются:

Развернутый анализ крови
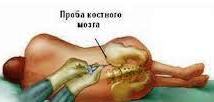
Биопсия костного мозга с последующим цитогенетическим исследованием (оценивается клеточный состав, степень фиброза, проводится цитохимическое исследование)
Цитогенетическое исследование клеток периферической крови и костного мозга, при возможности с помощью специфических проб
Определение щелочной фосфатазы нейтрофилов периферической крови (она снижена)
УЗИ органов брюшной полости (печень, селезенка, почки), при кожных поражениях биопсия с последующим иммуногистохимическим исследованием. Это позволяет определить распространенность и массу опухоли.
Чаще всего, хронический миелолейкоз диагностируется в хронической фазе.
Традиционный первый курс лечения – химиотерапия, который нормализует количество клеток. В отличие от трансплантации костного мозга, химиотерапия не обеспечивает полного излечения, хотя может вызывать длительные периоды ремиссии.
Химиотерапия является единственным методом лечения многих больных в таких случаях:
когда физическое состояние пациента не позволяет проводить трансплантацию и выдерживать высокодозную химиотерапию и лучевую терапию, предшествующую трансплантации.
когда пациенты выбирают химиотерапию, не желая подвергаться высокому риску, сопутствующему трансплантации. Терапия с участием интерферона вызывает ряд побочных эффектов, но, в целом, не является слишком агрессивным методом лечения и может существенно продлить жизнь пациента.
при отсутствии совместимого донора.
Терапию хронического миелолейкоза начинают с момента установления диагноза и обычно проводят амбулаторно.
В хроническую фазу болезни лечение направлено на снижение количества лейкоцитов и поражения периферических органов. Препаратами выбора обычно являются гидроксимочевина ( 10-20 мг/кг веса/сутки) или бусульфан/миелосан ( 4 мг/день). При неэффективности бусульфана возможна его комбинация с гидроксимочевиной или цитарабином, однако эффект от этого обычно невелик.
При значительном увеличении селезенки можно провести ее облучение.
Одним из новых препаратов в лечении хронического миелолейкоза является альфа-интерферон. Назначение его в дозе 59000000 ЕД трижды в неделю подкожно, внутрикожно или внутримышечно дает полные гематологические ремиссии у 70-80% больных, а цитогенетические ремиссии у 60% больных.
При переходе процесса в терминальную стадию используют комбинации цитостатических препаратов, обычно применяемых для лечения острых лейкозов: винкристин и цитозар, преднизолон и рубомицин.
В самом начале терминальной стадии иногда эффективен миелобромол.
Трансплантация костного мозга проводится больным моложе 50 лет в I стадии заболевания и в 70% случаев приводит к выздоровлению.
На фоне химиотерапии средняя продолжительность жизни составляет 57 лет. Смерть при хроническом миелолейкозе наступает в период бластного криза от инфекционных осложнений и геморрагического синдрома.
На прогноз существенно влияет наличие филадельфийской хромосомы и чувствительность заболевания к терапии. Использование альфа-интерферона существенно изменяет прогноз заболевания к лучшему.
